Saúde
Após decisão do STF, Anvisa pede ‘prazo justo’ de análise para vacinas

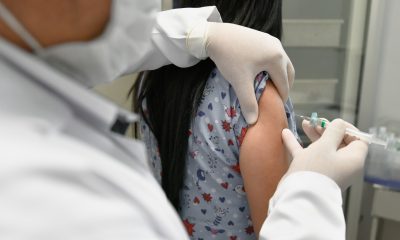
Diretores e técnicos da Agência Nacional de Vigilância Sanitária (Anvisa) defenderam um “prazo justo” para a análise de vacinas contra covid-19 após o Supremo Tribunal Federal (STF) permitir que estados e municípios comprem imunizantes aprovadas por entidades reguladoras de outros países. Eles também alertaram que a falta de aval do órgão brasileiro pode gerar dificuldades de monitoramento e fiscalização.

Conforme a decisão tomada hoje (23), quando a Anvisa não conceder autorização em 72 horas, a vacina poderá ser importada se já tiver o aval de agências reguladoras da Europa, dos Estados Unidos, do Japão ou da China. Segundo o entendimento da maioria dos ministros, essa compra poderá ocorrer se houver falha ou omissão do Ministério da Saúde na gestão do Plano Nacional de Imunização (PNI) ou se as doses disponibilizadas forem insuficientes para o combate à pandemia.
“Precisamos de um prazo para fazer uma análise mínima com critérios que são utilizados também por outras agências reguladoras. E é importante frisar que não pedimos um prazo justo porque queremos fazer retrabalho ou porque queremos ser burocráticos. A importância de ter um tempo adequado para a análise é porque existem questões específicas para o nosso país que precisam ser endereçadas. Existem compromissos que precisam ser feitos com a Anvisa”, disse Gustavo Mendes, gerente-geral de medicamentos e produtos biológicos da Anvisa.
A questão foi levantada nesta terça-feira durante coletiva de imprensa que apresentou detalhes da concessão do registro definitivo à vacina desenvolvida em parceria pela farmacêutica norte-americana Pfizer e pela empresa de biotecnologia alemã BioNtech. A análise levou 17 dias.
Estruturas de produção
Uma questão que preocupa o órgão é que as farmacêuticas possuem diferentes estruturas de produção. Assim, os lotes enviados ao Brasil podem não ser fabricados nos mesmos locais daqueles destinados a outros países.
“Temos casos em que o produto que vem para cá não é o mesmo que vai para os Estados Unidos. Cada uma dessas outras plantas fabris precisam ser avaliadas conforme os parâmetros das boas práticas de fabricação. Por isso é importante o nosso registro”, disse Ana Carolina Marino, gerente de Inspeção e Fiscalização de Produtos para a Saúde da Anvisa.
Ana alerta que, sem conhecimento dos detalhes da vacina que está sendo aplicada, haverá dificuldade para monitorar os resultados da vacinação e fiscalizar o produto. “Num contexto de fiscalização, se permitimos entradas de vacinas sem registro, em uma futura suspeita de falsificação, a Anvisa ficará completamente às cegas. Não conseguirá distinguir o que é um produto regular do que é irregular. É importante ter os dados para coibir fraudes”.
Responsabilização
Para Gustavo Mendes, a avaliação técnica não pode abrir mão do tempo necessário e do acesso aos dados. As farmacêuticas devem apresentar uma série de informações quando fazem o pedido de registro e, muitas vezes, há solicitação de complementação dos dados.
“Se não tivermos acesso aos dados para tomar uma decisão, como podemos nos responsabilizar? O ato do registro é uma responsabilização da área técnica. Apresentamos o que a gente viu e o que a gente não viu. E tudo isso irá compor o parecer que aponta se a vacina pode ser utilizada. Não entramos no mérito da questão legal ou política. O que precisamos é do mínimo de confiança técnica. Nós estamos sensíveis à situação da pandemia. De forma alguma queremos inviabilizar vacinas”, afirmou.
Edição: Fábio Massalli
Saúde
Saúde estadual alerta: vacinas evitam internações e mortes
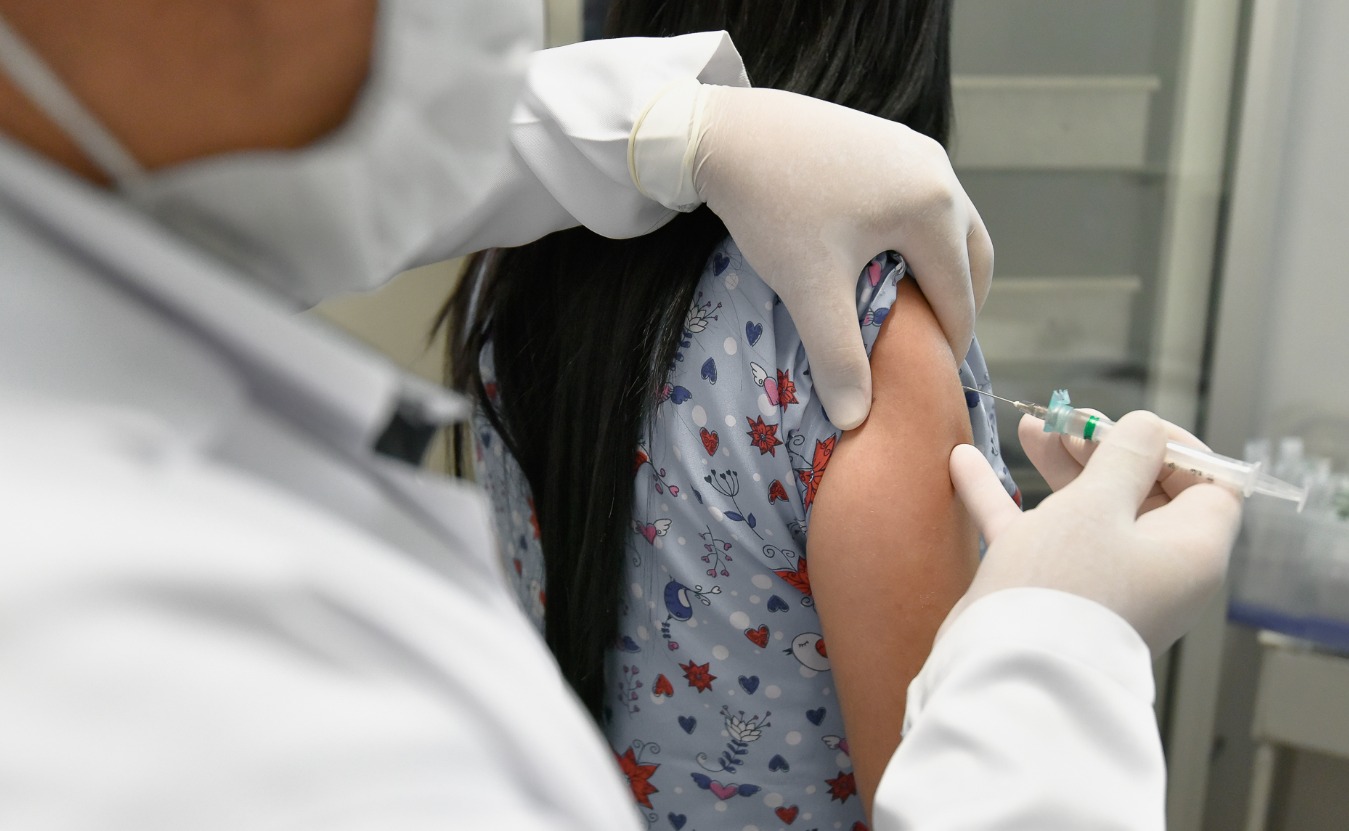
Secretaria de Saúde relata aumento de internações e mortes por dengue e influenza, principalmente entre idosos e crianças
Doenças como dengue e influenza em Goiás têm provocado aumento de diagnósticos e internações, com mais mortes. Desde o início do ano, já foram registrados mais de 150 óbitos por dengue. Já a Síndrome Respiratória Aguda Grave (Srag) resultou em 179 óbitos, principalmente entre crianças menores de 2 anos (16 mortes), e idosos com 60 anos. Dentre as principais causas, pode estar a baixa cobertura vacinal para dengue e Influenza.
A grande preocupação da Secretaria de Estado da Saúde de Goiás (SES-GO), no momento, é com a alteração da sazonalidade da dengue e doenças respiratórias, como a influenza, com as mudanças climáticas, que já começam neste mês. Segundo a superintendente de Vigilância em Saúde, Flúvia Amorim, o histórico de Srag mostra aumento de casos neste período, quando começam as inversões térmicas. “É nesta época que começam a circular os vírus respiratórios, de forma mais intensa”, explica.
Flúvia Amorim chama a atenção, principalmente, para os extremos das faixas etárias, que são crianças e idosos, as principais vítimas de doenças respiratórias. “Para essas pessoas, o quadro pode ser muito grave. Por isso, não deixem de se vacinar”, orienta. “Se você faz parte de algum dos grupos prioritários, procure rapidamente o posto de vacinação”, continua Flúvia, para lembrar que, embora haja vacina disponível contra a influenza em todos os postos de vacinação dos 246 municípios, apenas 20,82% do público-alvo (grupos prioritários) buscaram o imunizante. Já em relação a Covid-19, a cobertura vacinal está em 20,82%. “A vacina demora dez dias para fazer efeito. Então, quanto mais rápido se vacinar, mais rápido a pessoa estará protegida”, avisa.
A Superintendente de Regulação, Controle e Avaliação da SES, Amanda Limongi, também reforça a importância da vacinação. “É o meio mais eficaz de prevenir internações, tanto de dengue quanto de Síndromes Respiratórias Agudas Graves”, afirma, ao confirmar que o “encontro” de casos de dengue e doenças respiratórias tem demandado mais internações em Goiás.
Ela faz um apelo também à população dos municípios que ainda dispõem de vacinas contra a dengue. “Dos 246 municípios goianos, 155 ‘zeraram’ seus estoques, mas ainda faltam 10 mil doses a serem aplicadas”, explica. A superintendente se refere ao restante das 158,5 mil doses recebidas do Ministério da Saúde e que vão vencer em 30 de abril, mesmo com a ampliação da idade para pessoas de 4 a 59 anos. Essa ampliação vale apenas para esses lotes do imunizante. Para a próxima, já está definido o retorno das idades de 10 a 14 anos, para o público-alvo.
Fotos: Iron Braz / Secretaria de Estado da Saúde – Governo de Goiás
-

 Cidades12/05/2024
Cidades12/05/2024Mais de 20 mil profissionais ligados ao Governo Federal atuam diretamente no auxílio ao Rio Grande do Sul
-

 Geral14/05/2024
Geral14/05/2024Ministério da Saúde já enviou 25 toneladas de medicamentos e insumos para atender população gaúcha
-

 Nacional13/05/2024
Nacional13/05/2024“É um compromisso nosso deixar o Rio Grande do Sul como era antes da chuva”, diz Lula em reunião ministerial
-

 Nacional15/05/2024
Nacional15/05/2024Lula anuncia hoje quarta (15) novas medidas para ajudar a população e a reconstrução do RS
-

 Ação Social17/05/2024
Ação Social17/05/2024Governo promove ações de combate à exploração infantil no turismo